by Philip Stevens
Em um mundo onde os investidores podem escolher entre diferentes jurisdições, as economias de inovação bem-sucedidas devem ter estruturas de políticas de PI que vão além do mínimo fornecido pelo Acordo TRIPS.
Este artigo discute duas reformas que podem ajudar o Brasil a se tornar o líder latino-americano em Biociências.
A busca urgente do Brasil pelo crescimento
A economia do Brasil está em uma encruzilhada. A Covid-19 deixou cicatrizes econômicas, incluindo aumento da inflação, desemprego e desigualdade. O real se desvalorizou e o país perdeu grande parte de sua indústria nas últimas duas décadas, caindo de 26% do PIB em 1980 para 11% em 2018. A economia brasileira se tornou dependente das exportações de commodities, que estão propensas a forças globais imprevisíveis fora do controle de Brasília. A confiança dos investidores internacionais no país é frágil e deve ser reconstruída pelo novo governo.
Para criar empregos e para um crescimento econômico mais sustentável, o Brasil deve acelerar e consolidar sua transição econômica de manufatura básica e exportação de commodities para indústrias de maior valor e baseadas no conhecimento. Essas indústrias – incluindo biofarmacêuticos, tecnologia da informação, produtos químicos e entretenimento – sustentam o crescimento sustentável e o emprego nas economias de quase todos os países de alta renda, com a China também fazendo grandes esforços para reorientar seu modelo econômico nessa direção.
Para ter sucesso no futuro, o Brasil também deve impulsionar suas indústrias de inovação, mas isso requer o enquadramento político adequado. Juntamente com um ambiente regulatório, competente e fiscal favorável, uma área política chave, mas na maioria das vezes negligenciada, é a proteção dos direitos de propriedade intelectual (PI).
Uma estrutura de PI forte e previsível ajuda os empreendedores locais a garantir investimentos para suas inovações e a construir negócios viáveis. Empresas multinacionais intensivas em conhecimento, que trazem consigo habilidades, conhecimento e capital tão necessário, investirão no Brasil. Produtos de alta tecnologia serão lançados mais rapidamente, abrindo para os cidadãos todos os tipos de tecnologias de melhoria da saúde e da produtividade. Isso faz parte da receita para o crescimento econômico sustentável.
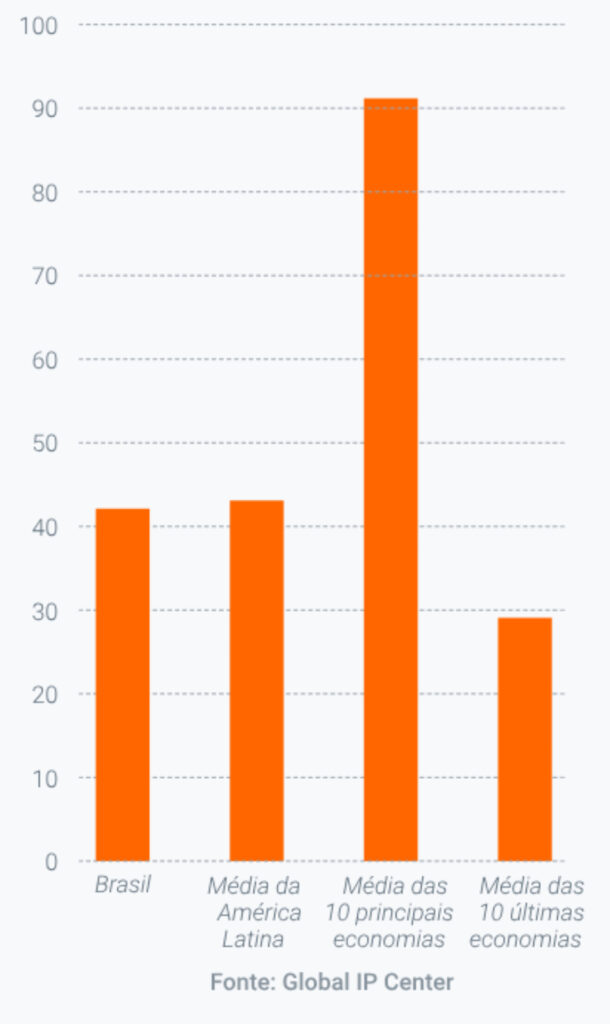
A administração anterior fez alguns movimentos para melhorar ainda mais o ambiente de PI para investidores, incluindo a criação de um novo Grupo Interministerial de Propriedade Intelectual para coordenar e supervisionar todas as questões relacionadas à política de PI no Brasil. No entanto, o Brasil ainda apresenta desempenho inferior ao das melhores economias do mundo em proteção de PI (Figura 1).
FIGURA 1: DESEMPENHO DO BRASIL NO GLOBAL IP INDEX 2022
Fonte: Global IP Center
Em um mundo onde o capital é volátil e os investidores podem facilmente escolher entre diferentes jurisdições, as economias de inovação bem-sucedidas devem ter estruturas de políticas de PI que vão além do mínimo fornecido pelo Acordo TRIPS.
Na verdade, para ser bem-sucedido na economia moderna, os países devem fornecer proteções de PI que atendam aos desenvolvimentos de novas tecnologias, ao mesmo tempo em que fornecem previsibilidade e certeza. Aqui, há duas reformas que beneficiariam o ambiente brasileiro de PI e o tornariam muito mais competitivo internacionalmente: proteção regulatória de dados para medicamentos; e legislação para garantir que os inventores aproveitem o prazo total de suas patentes.
Proteção de dados regulatórios
Na medicina, o domínio das drogas de moléculas pequenas está chegando ao fim. Os tratamentos futuros serão biológicos – drogas complexas com estruturas moleculares muitas vezes maiores, fabricadas dentro de estruturas vivas, como células animais ou bactérias.
A nova era da biotecnologia promete uma revolução na forma como os médicos lidam com as doenças, dando esperança a pacientes com doenças para as quais não há tratamento no momento. Os avanços na terapia genética, o desenvolvimento de vacinas mais seguras, a medicina de precisão e diagnósticos superiores beneficiam bilhões de pessoas.
A proteção de dados regulatórios (RDP) protege contra a divulgação de dados de teste e, durante um certo tempo, a confiança de terceiros em dados diretamente ou por referência. Essencialmente, a RDP impede que os concorrentes confiem indevidamente nos dados gerados em ensaios clínicos pelo desenvolvedor original do medicamento ou produto químico agrícola, que são obrigados a divulgar aos reguladores para obter aprovação regulatória para o novo produto.
Os ensaios clínicos estão se tornando cada vez mais caros e complicados e aumentam significativamente o custo de desenvolvimento de um novo medicamento ou produto químico. Na maioria dos setores, as empresas podem proteger os dados comercialmente sensíveis por meio de leis de sigilo comercial, mas a exigência de que as empresas biofarmacêuticas divulguem dados aos reguladores as coloca em desvantagem competitiva.
Um prazo suficiente de proteção de dados regulatórios, portanto, dá aos inovadores tempo suficiente para recuperar os custos de compilação de dados de ensaios clínicos antes de serem disponibilizados aos fabricantes de genéricos ou biossimilares para uso em seus próprios pedidos de aprovação de comercialização.
No caso dos medicamentos biológicos, a proteção dos dados de ensaios clínicos também é importante, já que as patentes sozinhas podem fornecer proteção insuficiente. Isso ocorre porque a estrutura molecular dos medicamentos biológicos é muito mais complexa do que os medicamentos “tradicionais” sintetizados quimicamente, tornando impossível replicar um medicamento biológico original com precisão. Tendo em vista que cada biossimilar é ligeiramente diferente do originador, as patentes podem oferecer apenas proteção limitada, pois as patentes são concedidas para invenções específicas e não cobrem as variações que inevitavelmente surgirão no processo de desenvolvimento de um biossimilar.
Por isso, os países mais inovadores em biotecnologia, produtos químicos e medicamentos veterinários têm regras claras e juridicamente vinculativas para proteger esses dados. Essa forma de direito de propriedade intelectual é particularmente importante para países que buscam ingressar na cadeia de valor de P&D através da disponibilização de ensaios clínicos e serviços correlatos – o Brasil é um bom exemplo disso.
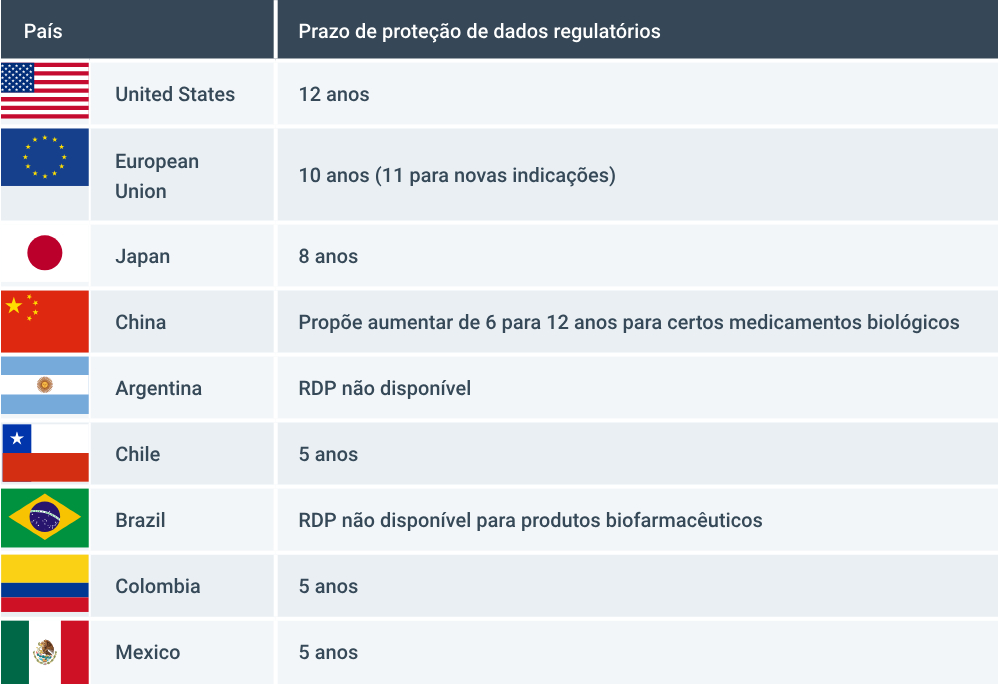
A proteção de dados regulatórios está disponível para inovadores nos países que lideram o investimento biofarmacêutico, sendo que a China está buscando aumentar seus padrões para melhorar a competitividade e a capacidade inovadora de sua economia (Figura 2)
FIGURA 2: PROTEÇÃO DE DADOS REGULATÓRios EM PAÍSES SELECIONADOS
Fonte: Managing IP / Geneva Network
Em 2002, o Brasil implementou a RDP para produtos veterinários, agrícolas e fertilizantes, excluindo explicitamente os biofarmacêuticos. Enquanto o Brasil procura melhorar sua competitividade internacional, o governo está debatendo se deve reverter essa posição e se juntar a muitos outros países que oferecem RDP.
O Brasil, historicamente, sempre relutou em oferecer RDP devido a preocupações com o acesso a medicamentos, com os oponentes argumentando que o fornecimento de RDP levaria a preços mais altos dos medicamentos e sobrecarregaria os orçamentos de saúde. Esses temores falham em olhar para o quadro geral e são infundados de acordo com um novo estudo da empresa de consultoria econômica Copenhagen Economics. Analisando os dados de 53 países ao longo de dez anos sobre essa questão, sua análise sugere que oferecer RDP pode trazer uma série de benefícios econômicos e de saúde pública.
A RDP aumenta a disponibilidade de medicamentos
O principal benefício da RDP é que ela traz medicamentos mais inovadores para um país, mais rapidamente. Os países com RDP comprovadamente têm mais medicamentos inovadores disponíveis, muito provavelmente porque a existência desse direito de propriedade intelectual oferece segurança aos inovadores e fortalece o caso de negócios para investir no lançamento de medicamentos em um novo mercado. A Copenhagen Economics constatou que os países com RDP têm uma disponibilidade média de 31,5% dos medicamentos lançados nos últimos cinco anos em comparação com apenas 11% de disponibilidade para países sem RDP – três vezes mais.
Utilizando esses dados, os pesquisadores estimam que o Brasil poderia aumentar em até 39% a disponibilidade de medicamentos inovadores se implementasse a RDP. Isso equivale a mais 570 medicamentos inovadores disponíveis no país. Isso poderia transformar a saúde no Brasil, com pacientes podendo se beneficiar de regimes de tratamento modernos que podem não estar disponíveis atualmente.
A evidência mostra que as regras da Proteção de Dados Regulatórios trazem mais medicamentos novos para um país e muito mais rápido.
A RDP tem impacto mínimo nos gastos com saúde
O Brasil tem relutado em implementar a RDP para os produtos biofarmacêuticos por causa da percepção de que isso aumentará os gastos com medicamentos e prejudicará os orçamentos da saúde pública. Os países que implementaram a RDP não constataram isso a longo prazo de acordo com a análise da Copenhagen Economics. No geral, os países que implementaram a RDP descobriram que os gastos com saúde de fato aumentaram marginalmente no curto prazo, mas se estabilizaram em sua trajetória de crescimento original após cinco a dez anos. Três razões são sugeridas para esse padrão:
- O mais óbvio é que a implementação da RDP não estendeu o período de proteção para a maioria dos medicamentos atualmente disponíveis. No Brasil, os pesquisadores constataram que 85% dos medicamentos tinham um prazo de patente restante de pelo menos cinco anos, o que significa que a implementação de RDP de cinco anos não teria nenhum impacto com a entrada dos genéricos para esses medicamentos inovadores. Isso significa que a entrada dos genéricos continua a exercer uma pressão para baixo sobre os custos de saúde.
- Os países que têm RDP têm medicamentos mais inovadores disponíveis para seus sistemas de saúde. O gasto com esses medicamentos pode levar a uma economia geral significativa do sistema de saúde à medida que os pacientes abandonam os tratamentos mais antigos e menos eficazes. Isso pode significar menos visitas às unidades de saúde, menos cirurgias e internações. É importante ressaltar que pacientes mais saudáveis podem reingressar na força de trabalho, aumentando a criação de riqueza e reduzindo os gastos com assistência social.
- Os gastos com saúde são controlados pelo governo, sendo que os governantes irão alocar os recursos de acordo com as necessidades e prioridades locais, independentemente das modificações no sistema de PI. O Japão e o Canadá implementaram a RDP em 2007 e 2006, respectivamente. Desde então, os gastos com medicamentos como percentual dos gastos gerais com saúde se mantiveram estáveis.
A RDP impulsionará a indústria brasileira de medicamentos genéricos e biossimilares
O Brasil tem uma grande e próspera indústria de genéricos que atende grande parte da demanda local e exporta regionalmente. Para evitar a estagnação, esse setor conta com um fluxo contínuo de lançamentos de medicamentos inovadores e a eventual expiração de seus direitos de propriedade intelectual. Quando um medicamento se torna disponível para a concorrência genérica, os fabricantes de genéricos contam com os investimentos feitos no lançamento desses produtos, especialmente os valiosos dados de ensaios clínicos que devem ser submetidos aos reguladores para obter a autorização de mercado.
Para o Brasil, a Copenhagen Economics estima que a implementação de RDP traria grandes benefícios para a indústria local. Sua análise sugere que a RDP aumentaria a disponibilidade de medicamentos inovadores em 34-39% em comparação com o nível atual. Com o tempo, após a expiração dos prazos de proteção da PI, 3,17 medicamentos genéricos ou biossimilares poderão ser disponibilizados no Brasil para cada medicamento inovador disponível. Isso sugere que a RDP, com o passar do tempo, é uma oportunidade de crescimento, não uma ameaça, para fabricantes de genéricos e biossimilares no Brasil.
O Brasil poderia aumentar em 138% o número de ensaios clínicos com a implementação da proteção de dados regulatórios
Mais ensaios clínicos acontecerão no Brasil
Um benefício final da implementação da RDP no Brasil é seu potencial para aumentar o Investimento Estrangeiro Direto, uma consideração crucial para um governo que busca enfrentar os desafios econômicos domésticos. Em especial, é provável que a implementação da RDP impulsione o investimento em ensaios clínicos, que, além de fornecer IED, também oferece uma série de benefícios ao sistema de saúde local. À medida que mais dados de ensaios clínicos são produzidos no Brasil, os medicamentos poderão ser mais bem integrados aos pacientes, médicos, centros de pesquisa, instituições acadêmicas e agências governamentais brasileiras.
O estudo da Copenhagen Economics conclui que os mercados com RDP têm em média 21 ensaios clínicos por milhão de habitantes, enquanto os mercados sem RDP têm em média 4. Isso significa uma diferença de 17 ensaios clínicos por milhão de habitantes. Para o Brasil, sua análise estatística mostra que o número médio de ensaios clínicos no Brasil poderia aumentar em 138%, de 445 atualmente para 1.059 com a implementação da RDP.
Esse aumento na atividade de ensaios clínicos facilitaria os investimentos de empresas internacionais. Além do mais, a gestão de ensaios clínicos é um passo importante na transição para a inovação biofarmacêutica novamente para as empresas farmacêuticas locais, contribuindo para a P&D e para a riqueza que essa atividade traz.
Ajuste do prazo de patentes
Como membro do Acordo TRIPS da Organização Mundial do Comércio, o Brasil se comprometeu a conceder patentes por um prazo de vinte anos (a partir da data do depósito). Para receber uma patente, os inventores devem divulgar publicamente sua invenção em troca de um direito exclusivo temporário à invenção – equilibrando a necessidade de incentivar os inventores a investir e comercializar novas tecnologias com a necessidade da sociedade por tecnologias novas e acessíveis. Esse contrato social está no cerne do sistema de patentes, impulsionando a inovação e a concorrência ao permitir que outros inventem e melhorem o produto, ao mesmo tempo em que garantem benefícios para a sociedade.
Na prática, poucas invenções no Brasil chegam perto desse prazo de proteção de vinte anos. O prazo de vinte anos começa a contar a partir do momento do depósito no escritório de patentes. No entanto, atrasos e backlogs enquanto o escritório de patentes (INPI) examina cada patente significa que leva em média 6,9 anos para que as patentes sejam concedidas.
Esse atraso médio de 6,9 anos (que é mais longo em certos setores) tira efetivamente a confiança em uma patente, privando assim o proprietário do prazo total. Embora um inovador possa começar a vender um produto enquanto sua patente está pendente, a realidade é geralmente bem diferente. As startups geralmente têm dificuldade de assegurar o investimento necessário para construir um negócio a menos ou até que uma patente seja concedida. Empresas ainda maiores hesitam em desenvolver um mercado até que saibam que obtiveram proteção de patente. Além disso, embora a lei brasileira permita processos por violação ocorrida antes da concessão da patente, há um prazo de prescrição de 5 anos – menor do que o atraso médio de 8 anos.
Além disso, esse atraso está fora dos padrões internacionais. Os escritórios de patentes nos EUA, China, Coreia, Europa e outras economias levam em média de 2 a 4 anos. Na verdade, as reformas de 2019 no Brasil estabeleceram 2 anos como meta.
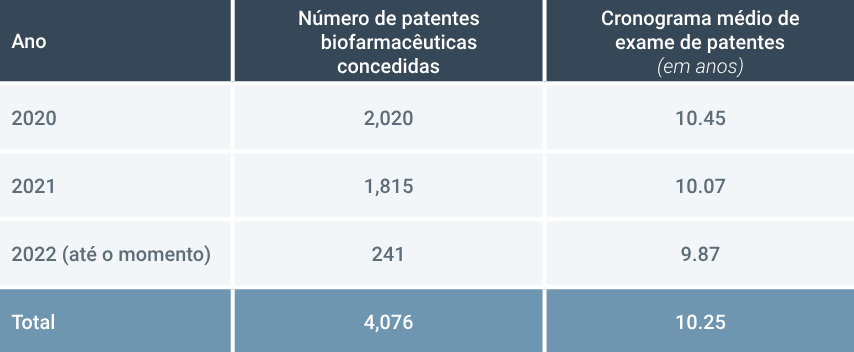
Os atrasos em certas áreas da tecnologia, como os biofarmacêuticos, são particularmente graves. A análise de Osha Bergman Watanabe & Burton LLP (Osha), mostra que o prazo médio de exame de patentes no Brasil é de 10,25 anos para as patentes biofarmacêuticas concedidas entre 2020 e 2022 (Figura 3).
FIGURA 3: PATENTES BIOFARMACÊUTICAS CONCEDIDAS DE 1º DE JANEIRO DE 2020 A 23 DE MARÇO DE 2022
Além disso, o problema de pendências de exames de patentes biofarmacêuticas no Brasil mostra sinais de agravamento, com cerca de 13.688 patentes biofarmacêuticas pendentes em março de 2022, de acordo com a Osha. Apesar disso, a taxa de exame pelo INPI parece estar diminuindo, com o número de patentes examinadas e concedidas desde 2020 diminuindo a cada ano de 2.020 em 2020 para 1.815 em 2021 para uma estimativa de 1.400 em 2022 (com base no número processado até o momento).
Anteriormente, alguma compensação por tais atrasos no exame das patentes era garantida pelo Artigo 40 de um prazo de patente de 10 anos. Mas a decisão de maio de 2021 do Supremo Tribunal, declarando que o Artigo 40 é inconstitucional para todas as tecnologias e aplicando a decisão retrospectivamente apenas a produtos farmacêuticos e outras invenções relacionadas à saúde, remove esse importante respaldo do regime de PI do Brasil.
A decisão deixa os inovadores no Brasil trabalhando com um sistema de patentes que atribui pouco valor às suas invenções, colocando o país muito abaixo dos padrões de PI dos países com os quais tenta competir por investimentos. Por exemplo, o tempo médio para conceder uma patente é de 2,8 anos na Coreia, 2,9 anos na China e menos de 2 anos nos Estados Unidos, o que significa que os inovadores desses países desfrutam de uma vida útil de patente muito mais longa.
Atrasos no exame de patentes prejudicam a economia e a sociedade
O demorado sistema de exame de patentes do Brasil prejudica sua economia de várias maneiras.
- Primeiro, os atrasos no exame de patentes prejudicam os empresários e minam a capacidade de novos negócios se desenvolverem e crescerem. As startups dependem de investimentos externos, e os investidores geralmente querem ver as patentes para assegurar seus investimentos. A pesquisa mostra que cada ano de atraso reduz as vendas das startups, os níveis de emprego e a probabilidade de abrir o capital com uma oferta de ações.
- Segundo, os atrasos também prejudicam a sociedade. De acordo com o Escritório de Propriedade Intelectual do Reino Unido, as perdas combinadas de backlogs apenas no Escritório de Patentes e Marcas dos EUA, no Escritório de Patentes do Japão e no Escritório Europeu de Patentes custam à economia global mais de 10 bilhões de dólares por ano devido à perda de investimentos, empregos e produtos.
- Por último, os atrasos no escritório de patentes prejudicam os consumidores e pacientes ao atrasar a entrada no mercado de novos produtos, tecnologias e tratamentos médicos. Isso é especialmente verdade no caso dos medicamentos, onde a pesquisa mostrou uma ligação entre o atraso na disponibilidade de novos medicamentos e a proteção de patente fraca. Esses atrasos no lançamento não surpreendem, tendo em vista os investimentos significativos que precisam ser feitos em cada novo mercado para aprovação regulatória, desenvolvimento de infraestrutura e educação médica para cada novo medicamento. Se a concessão de uma patente atrasar, esses investimentos não começarão até que a patente seja concedida, o que significa um acesso mais lento a novos medicamentos.
Além disso, para que o sistema de patentes atinja seus objetivos econômicos e sociais e proporcione um ambiente favorável à inovação, ele precisa ser estável e previsível. O exame rápido de patentes é fundamental para isso.
Em 2019 foi anunciada uma nova iniciativa, o Plano de Combate ao Backlog de Patentes. O INPI aprovou várias resoluções administrativas nos últimos anos, todas com o objetivo de acelerar a tomada de decisão e o processo de processamento de patentes para pedidos com e sem buscas e documentação existentes do estado da técnica.
Embora isso sinalize vontade política, eles não incentivam o escritório de patentes a acelerar seus processos, nem fornecem compensação aos detentores de direitos que sofrem com a erosão dos prazos da patente sem terem culpa.
Por que o ajuste no prazo das patentes é importante
Para resolver o problema do demorado exame de patentes, um número crescente de países tem mecanismos para restaurar uma parte da patente perdida devido a atrasos injustificados no exame, comumente conhecido como Ajuste do Prazo de Patentes (PTA). Essa é uma reforma que o Brasil deveria considerar seriamente para restaurar a vida das patentes na ausência do parágrafo único do Artigo 40, e garantir que o sistema brasileiro de patentes seja comparável a seus pares internacionalmente. Ela iria diferir do artigo 40, na medida em que se aplicaria caso a caso, fornecendo um ajuste com base em qualquer atraso injustificado experimentado pelo (e não por culpa do) requerente em particular.
O PTA para atrasos nos escritórios de patentes está sendo usado por escritórios de patentes em todo o mundo, incluindo os membros da OCDE (Chile, Colômbia, Costa Rica, México, Coreia e Estados Unidos). Embora os esquemas difiram em seus detalhes precisos, todos eles empregam várias fórmulas para calcular o período de vida da patente que deve ser restaurado devido a atrasos no processo de exame da patente que não são culpa do depositante. Dessa forma, os esquemas de PTA garantem que a vida útil da patente seja significativa, dando segurança e estabilidade para os inovadores e, em última análise, ajudando o sistema de patentes a cumprir seu papel social e econômico pretendido.
O Chile, membro da OCDE e vizinho regional, por exemplo, conta com padrões mais elevados em muitas áreas de seu sistema de patentes, incluindo a provisão de Ajuste do Prazo de Patentes para compensar atrasos no exame de patentes. Graças a essa e outras medidas, os inovadores no Chile contam com tempos médios de exame muito mais rápidos, de aproximadamente quatro anos (ainda não é perfeito, mas é bem melhor do que os 6,9 do Brasil). Desde 1º de junho de 2021, as emendas à lei de patentes da China que implementam esse sistema entraram em vigor, mostrando a seriedade com que o assunto é levado por países que priorizam a inovação.
O Ajuste do Prazo de Patentes é semelhante, mas diferente da Extensão do Prazo de Patentes (Certificados Suplementares de Proteção na UE), que restauram a vida útil das patentes biofarmacêuticas causadas por atrasos no processo de aprovação regulatória. Enquanto a Extensão do Prazo de Patentes está disponível apenas para medicamentos, o Ajuste do Prazo de Patentes está disponível para patentes de todas as formas de tecnologia. É importante observar que o PTA não constitui uma extensão da vida da patente, mas sim uma restauração parcial do tempo perdido com atrasos burocráticos.
O Ajuste do Prazo de Patentes existe em todo o mundo, inclusive nos membros da OCDE (Chile, Colômbia, Costa Rica, México, Coreia e Estados Unidos).
Conclusão
Tendo em vista sua base científica existente, a biodiversidade e os pontos fortes em produtos farmacêuticos e outras formas de fabricação de alta tecnologia, o Brasil está bem-posicionado para se reorientar para uma economia de conhecimento de alto valor. Uma estrutura robusta e previsível para a proteção dos direitos de propriedade intelectual será fundamental para essa transformação.
Muito está em jogo. O Brasil anunciou sua intenção de ingressar na OCDE, uma conquista que confirmaria o país como um dos principais destinos de investimentos, beneficiando-se de altos padrões de governança. Esse processo exigirá reformas profundas em várias áreas de governança, incluindo a estrutura para a proteção dos direitos de propriedade intelectual.
O Brasil possui alguns princípios básicos de PI, mas os governantes brasileiros reconhecem que, na competição global por investimentos, padrões mínimos ou abaixo da média de PI não são suficientes. O Brasil deve se tornar atraente tanto para inovadores internacionais quanto nacionais. Melhorar a proteção de PI para a próxima geração de medicamentos biológicos via RDP e fornecer garantias legislativas sobre a vida útil significativa das patentes via PTA são duas reformas simples que podem fazer o Brasil se destacar no meio da multidão e garantir sua competitividade internacional.